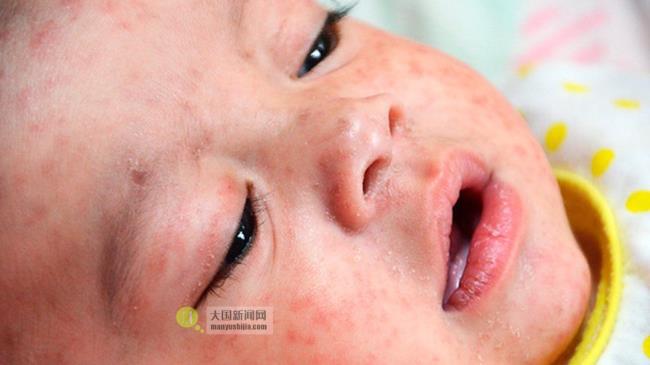
北卡罗来纳大学医学院的科学家在《JCI Insight》杂志上报告了一种针对安琪尔曼综合征的基因治疗策略的早期测试。安琪尔曼综合征是一种神经发育障碍,其特点是肌肉控制和平衡能力差,难以治疗的癫痫和智力障碍。
每2万名儿童中就有1名患有安琪尔曼综合症,仅在美国就有超过1.5万人患有此病。没有特效治疗方法,但是科学家由Ben Philpot博士基南特聘UNC细胞生物学和生理学教授医学院和北卡罗来纳大学神经科学中心副主任,之前建议治疗疾病最好的方法就是恢复UBE3A基因功能神经元,这在患有安琪尔曼综合症的人的大脑中已经消失了。
天使综合征的遗传学比典型的单基因疾病如囊性纤维化和镰状细胞性贫血更为复杂。人类的大多数基因都继承了一个母亲和一个父亲的副本。Angelman综合征发生在母亲的UBE3A拷贝因某种原因发生突变或缺失的儿童身上。由于尚未完全清楚的原因,成熟的神经元通常只表达UBE3A的母副本;父亲的拷贝被有效地沉默了。因此,当母体拷贝丢失时,该基因的功能在神经元中就消失了。由于UBE3A编码的一种蛋白质有助于调节其他重要蛋白质的水平,它的缺失会严重破坏大脑发育。
复杂的是,神经元表达了UBE3A的两种不同变体或“异构体”,它们的长度略有不同——一种短型和一种长型——比例约为三种短型对应一种长型。
Philpot的团队能够制作出一个版本的UBE3A,当神经元表达时,可以以接近正常的比例产生短和长形式的UBE3A蛋白。科学家们将治疗用的UBE3A基因插入到一种病毒衍生的载体中,或称“载体”,这种载体被设计成可以可靠地传递给神经元。他们将这种载体的溶液注入新生Angelman综合症模型小鼠大脑的中空空间(称为脑室),这些小鼠缺乏母鼠Ube3a基因的复制体。就像患有安琪尔曼综合征的人类一样,这些小鼠的神经元中不能表达UBE3A蛋白,并在生命的最初几个月里出现运动障碍、癫痫和其他神经症状。
Philpot和他的同事证实,载体携带的UBE3A在注射后几天就在Angelman模型小鼠大脑的神经元中变得活跃,其水平与正常基因相似。这种治疗恢复了运动技能学习和老鼠挖掘、挖洞和筑巢的基本行为。未经治疗的小鼠出现了常见的安琪尔曼样损伤。与未接受治疗的小鼠相比,接受治疗的小鼠对实验诱发的癫痫发作也不那么敏感,重要的是,它们没有遭受任何明显的负面副作用。

马修贾德森博士
“这是一个概念验证研究,但是如果这些早期的结果翻译诊所,他们将代表大改进:Angelman综合征患者的生活质量,”研究报告的主要作者Matt贾德森博士Philpot实验室的研究助理,执行大部分的实验。
研究人员计划进一步发展他们的策略,首先在老鼠和猴子身上进行更多的测试,以优化剂量和给药方法,最后,在有希望的安全结果出现之前,进行人类临床试验。如果这种疗法可行,研究人员预计,它可能对任何年龄的人都有好处,但可能有不同的好处。
菲尔波特说:“从出生到四年的范围可能是理想的,但我们认为,只要我们能恢复这种基因在大脑中的功能,我们就可能看到一些改善。”
与贾德森和菲尔波特(最近被列为世界领先的天使综合征研究人员)一起,《JCI Insight》的论文由查尔斯·申格(Charles Shyng)、杰里米·西蒙(Jeremy Simon)、考特尼·戴维斯(Courtney Davis)、马蒂斯·庞特(Mattijs Punt)、米拉贝尔·萨蒙(Mirabel Salmon)、诺亚·米勒(Noah Miller)、金伯利·里托拉(Kimberly Ritola)、Ype Elgersma、大卫·阿马拉尔(David Amaral)和史蒂文·格雷(Steven Gray)共同撰写。
该研究得到了安琪曼综合征基金会(Angelman Syndrome Foundation)和美国国立卫生研究院(National Institutes of Health)的支持(R01HD093771, r01mhh120229, R01NS114086)。